-
(유기화학) 극성 용매 vs 비극성 용매 | 양성자성 용매 vs 비양성자성 용매 | 개념과 예시 알아보기이슈 & 정보 2025. 2. 7. 18:03728x90300x250
극성 용매와 비극성 용매, 양성자성 용매와 비양성자성 용매는 화학 반응 및 용해 과정에서 결정적인 역할을 하는 핵심 개념입니다.
이들의 차이점과 특성을 이해하면 유기 화학 반응 메커니즘을 해석하고 실험 조건을 최적화하는 데 도움이 됩니다.1. 극성 용매 vs 비극성 용매
1.1 정의와 분자 구조
극성 용매는 분자 내 전하 분포가 불균일하며 쌍극자 모멘트가 큰 액체입니다. 전기 음성도 차이가 큰 원자(예: O, N)가 결합되어 부분 전하(+δ/-δ)가 발생합니다. 반면, 비극성 용매는 전하 분포가 균일하고 쌍극자 모멘트가 없거나 매우 작은 액체입니다. 주로 탄소-수소(C-H) 결합으로 구성됩니다.
극성 용매와 비극성 용매의 주요 특성을 비교해보면, 전하 분포 측면에서 극성 용매는 불균일한 반면 비극성 용매는 균일합니다. 쌍극자 모멘트의 경우 극성 용매는 큰 값을 가지지만, 비극성 용매는 없거나 매우 작습니다. 분자간 힘에 있어서 극성 용매는 수소 결합과 쌍극자-쌍극자 상호작용이 주요하게 작용하는 반면, 비극성 용매는 주로 반데르발스 힘이 작용합니다. 유전 상수의 경우 극성 용매는 높은 값을 가지며(예: 물의 유전 상수는 약 80), 비극성 용매는 낮은 값을 가집니다(예: 헥산의 유전 상수는 약 1.9).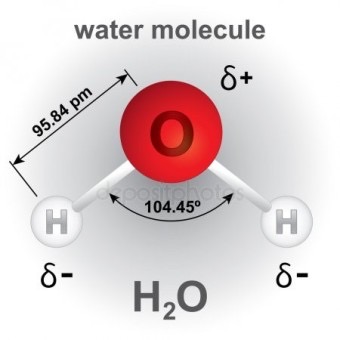
물분자 구조 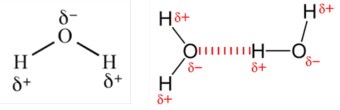
1.2 용해 특성
극성 용매는 이온성 화합물(NaCl)이나 극성 분자(설탕)를 잘 용해시킵니다. 예를 들어, 물에 소금이 녹을 때 Na⁺와 Cl⁻ 이온이 물 분자의 전하에 의해 안정화됩니다. 반면, 비극성 용매는 지방, 왁스, 탄화수소 등 비극성 물질과 잘 혼합됩니다. 예를 들어, 헥산은 기름을 용해하지만 물과는 층 분리가 발생합니다.
1.3 대표적 예시
극성 용매의 대표적인 예로는 물(H₂O), 에탄올(C₂H₅OH), 아세톤((CH₃)₂CO)이 있습니다. 비극성 용매의 예로는 벤젠(C₆H₆), 톨루엔(C₇H₈), 헥산(C₆H₁₄)이 있습니다.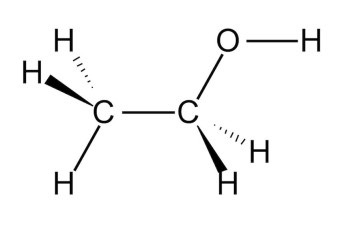
에탄올 구조 
아세톤 구조 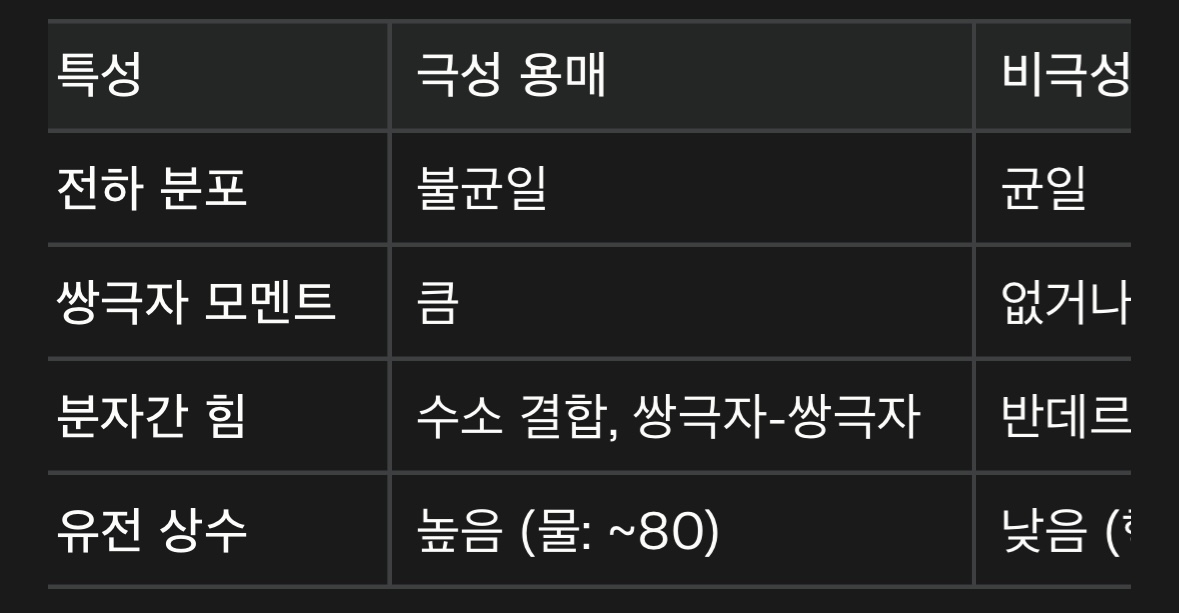

톨루엔 구조 2. 양성자성 용매 vs 비양성자성 용매
2.1 정의와 화학적 특성
양성자성 용매는 O-H 또는 N-H 결합을 포함하여 수소 이온(H⁺)을 제공할 수 있는 극성 용매입니다. 예를 들어, 물은 H⁺를 방출하여 산성 환경을 생성할 수 있습니다. 반면, 비양성자성 용매는 O-H/N-H 결합이 없어 H⁺를 제공하지 않는 극성 용매입니다.
양성자성 용매와 비양성자성 용매의 주요 특성을 비교해보면, H⁺ 제공 가능성 측면에서 양성자성 용매는 가능한 반면 비양성자성 용매는 불가능합니다. 수소 결합 형성 능력에 있어서도 양성자성 용매는 가능하지만 비양성자성 용매는 불가능합니다. 반응 유형 측면에서 양성자성 용매는 SN1 반응을 촉진하는 경향이 있고, 비양성자성 용매는 SN2 반응을 촉진하는 경향이 있습니다.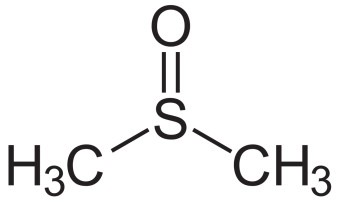
DMSO 구조 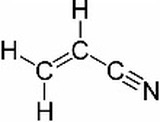
Acetonitrile 구조
2.2 반응 메커니즘 영향
SN1 반응의 경우, 양성자성 용매가 카보카티온 중간체를 안정화시켜 반응 속도를 증가시킵니다. 예를 들어, 물이나 에탄올에서 tert-부틸 클로라이드의 가수분해 반응이 이에 해당합니다. SN2 반응의 경우, 비양성자성 용매가 친핵체의 활성을 높여 이단자 치환 반응을 가속화합니다. 예를 들어, 아세톤에서 메틸 브로마이드와 하이드록시드 이온의 반응이 이에 해당합니다.
2.3 대표적 예시
양성자성 용매의 대표적인 예로는 물(H₂O), 메탄올(CH₃OH), 아세트산(CH₃COOH)이 있습니다. 비양성자성 용매의 예로는 디메틸설폭사이드(DMSO), 디메틸포름아미드(DMF), 아세토니트릴(CH₃CN)이 있습니다.
3. 화학 공학적 응용 사례
3.1 추출 공정
극성/비극성 용매 조합의 예로, 커피에서 카페인을 추출할 때 물(극성)과 디클로로메탄(비극성)을 사용합니다. 극성 용매가 카페인을 용해시키고 비극성 용매가 불순물을 제거합니다.
3.2 중합 반응
비양성자성 용매 사용의 예로, DMF에서 아크릴로니트릴 중합 시 극성 환경이 단량체의 용해도와 반응성을 향상시킵니다.
3.3 전기 화학 셀
유전 상수 조절의 예로, 리튬이온 배터리 전해액에 EC(에틸렌 카보네이트, 극성)와 DMC(디메틸 카보네이트, 비극성)를 혼합하여 이온 전도도를 최적화합니다.4. 용매 선택 시 고려 요소
1. 용질 극성: "유사한 용매가 유사한 용질을 녹인다"는 유사 용해 유사 원리를 적용합니다.
2. 반응 메커니즘: SN1/SN2 경로에 따라 용매 유형을 결정합니다.
3. 안전성: 벤젠(발암성) 대신 톨루엔 사용하는 추세입니다.
4. 환경 영향: 생분해성 용매(예: 초임계 CO₂) 개발이 확대되고 있습니다.
이러한 원리는 약품 제조, 폐수 처리, 신소재 합성 등 화학 공학 전 분야에서 활용되며, 용매의 물리화학적 특성을 이해하는 것이 공정 설계의 핵심입니다.728x90반응형'이슈 & 정보' 카테고리의 다른 글
(화학분석) 다공성물질의 기공과 비표면적 개념 | BET 분석방법 (0) 2025.02.08 에스터화 반응 | Esterification reaction | 에스터화 메커니즘 | 실험적 사례 (0) 2025.02.08 명리학의 기본 이론과 개념 | 음양오행 사주팔자 | 명리학 입문 (0) 2025.02.07 인도 배터리 전기차 시장 | LG에너지솔루션 현대자동차 인도 진출 배경 | 인도에 특허 출원으로 기술보호 전략 (1) 2025.02.07 비트코인 발행량 증가가 불가능한 이유 (0) 2025.02.06